Patógenos poscosecha y eficacia in vitro de PERIMAX® en kion (Zingiber officinale) de la Selva Central, Perú

El cultivo de jengibre (Zingiber officinale) es de alta relevancia económica y alimentaria, y en la etapa de poscosecha su calidad se ve fuertemente condicionada por la comunidad fúngica presente en los rizomas y en las condiciones de almacenamiento, la cual influye directamente en la aparición y progreso de pudriciones y marchitez poscosecha (Choi et al., 2024). En este contexto, hongos como Rhizoctonia spp., Fusarium spp. y Rosellinia spp. se reportan como taxones dominantes y agentes causales de “rhizome wilt”, asociados a pérdidas significativas de calidad y vida útil del producto durante el almacenamiento (Kaufman, 2016).
Por ello, resulta prioritario evaluar desinfectantes y formulados como PERIMAX® (ácido peracético 15%) frente a los patógenos prevalentes en rizomas de jengibre mediante ensayos in vitro que cuantifiquen la inhibición del crecimiento micelial y definan concentraciones efectivas para el control preventivo en lavado y desinfección, así como para el manejo sanitario en la etapa de poscosecha (Zendrato et al., 2024); en ese marco, el presente ensayo tuvo como objetivo evaluar la eficacia in vitro del ácido peracético 15% (PERIMAX ®) sobre el crecimiento micelial de Rhizoctonia spp. y Rosellinia spp., aislados de kion procedentes de diferentes packing de la Selva Central del Perú, mediante la técnica de medios envenenados a distintas concentraciones del producto.
METODOLOGÍA
Los aislamientos del patógeno se obtuvieron a partir de rizomas de kion con síntomas de mohos (blanco, gris y negro) colectados postcosecha en packings de la zona de Pichanaki, Selva Central del Perú, los cuales fueron desinfectados superficialmente, disecados en la zona de avance de la lesión y sembrados en medio PDA (Papa Dextrosa Agar) para su purificación e identificación morfológica presuntiva como Rhizoctonia spp. y Rosellinia spp. En la etapa de evaluación in vitro se prepararon medios PDA en placas Petri de 90 mm, incorporando PERIMAX® (ácido peracético 15 %) en el agar fundido (~35 °C) hasta obtener concentraciones finales de 0 (testigo), 100, 200, 300 y 400 ppm, de acuerdo con el esquema de dosificación establecido.
Cada tratamiento se inoculó en el centro con un disco de micelio activo y se incubó a 25,4 °C durante 3 días, registrando el crecimiento radial micelial hasta que el testigo alcanzó el borde de la placa. El efecto del desinfectante se expresó como porcentaje de inhibición del crecimiento micelial, calculado mediante la fórmula de Vincent (1947) a partir de los diámetros de crecimiento en el control (Dc) y en cada tratamiento (Dt).
A partir de las disecciones realizadas en diferentes partes del kion (particularmente de la zona donde se presentaba la sintomatología/ signo de moho blanco y moho gris) y sembradas en medio PDA, se encontraron diferentes microorganismos, entre las más comunes algunas bacterias y hongos.
EFICACIA IN VITRO
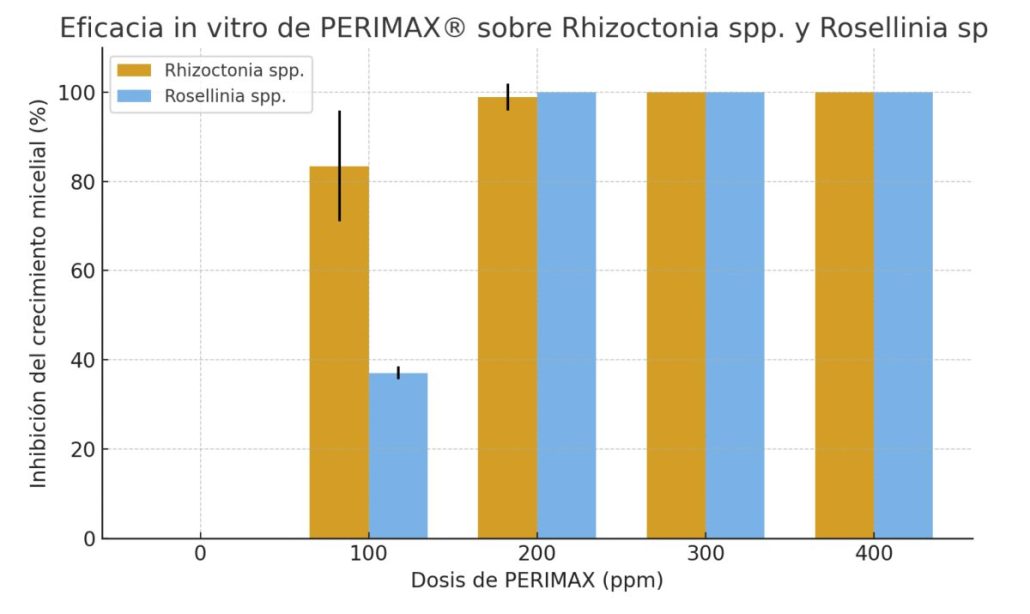
El análisis de varianza mostró diferencias altamente significativas entre las dosis de ácido peracético para ambos patógenos, evidenciando un efecto directo y marcado de PERIMAX® sobre el crecimiento micelial. En Rhizoctonia spp., el ANOVA indicó un efecto altamente significativo de la dosis (F = 374.2; p < 0.0001), con una reducción drástica del crecimiento micelial a medida que aumentó la concentración: a 100 ppm se obtuvo una inhibición promedio del 83.4 %, mientras que a partir de 200 ppm la inhibición superó el 98 %, alcanzándose control total (100 %) desde 300 ppm. La prueba de Tukey confirmó diferencias significativas entre el testigo y todas las dosis tratadas, así como entre 100 ppm y ≥200 ppm, sin diferencias entre 200, 300 y 400 ppm, lo que sugiere que el umbral de eficacia máxima se logra desde 200 ppm. En Rosellinia spp., el ANOVA evidenció también diferencias extremadamente significativas entre tratamientos (F = 35 349; p < 0.001), con un patrón de respuesta similar pero con menor variabilidad: a 100 ppm se obtuvo una inhibición parcial del 37.1 %, mientras que a partir de 200 ppm se logró inhibición completa (100 %) que se mantuvo hasta 400 ppm, presentando una desviación estándar mucho menor a 100 ppm (DE = 1.41) que en Rhizoctonia (DE = 12.40). La prueba de Tukey corroboró diferencias significativas entre el control y todas las dosis tratadas, así como entre 100 ppm y las concentraciones ≥200 ppm, que no difirieron entre sí, confirmando que 200 ppm constituye una dosis efectiva para lograr control total del crecimiento micelial en ambas especies.
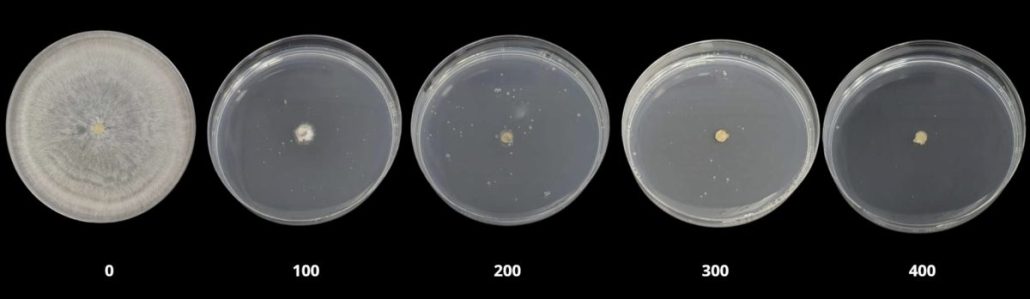
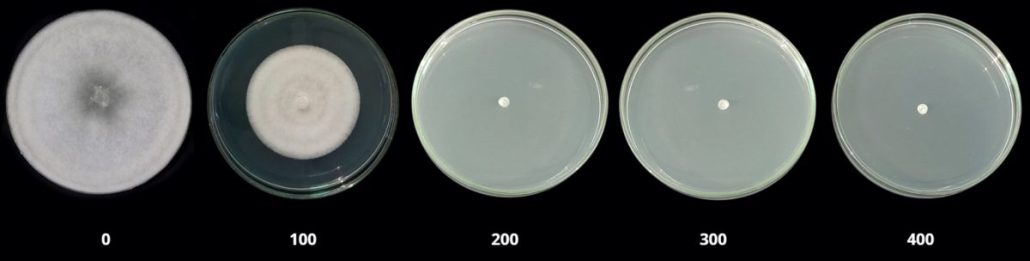
En la Figura 1 se presenta la inhibición porcentual del crecimiento micelial de Rhizoctonia spp. y Rosellinia spp. en función de la dosis de PERIMAX® (ácido peracético 15 %). Se observa un incremento marcado de la eficacia con la dosis, alcanzándose inhibición completa (100 %) a partir de 200 ppm en ambos patógenos, con diferencias en el patrón de respuesta inicial: a 100 ppm, Rhizoctonia spp. presentó una inhibición promedio superior (≈83 %) en comparación con Rosellinia s pp. (≈37 %). L as barras de error corresponden a la desviación estándar de las repeticiones. Se presentan las imágenes de las colonias en placa con medio de cultivo PDA y estructuras microscópicas (400X) observadas.
CONCLUSIONES
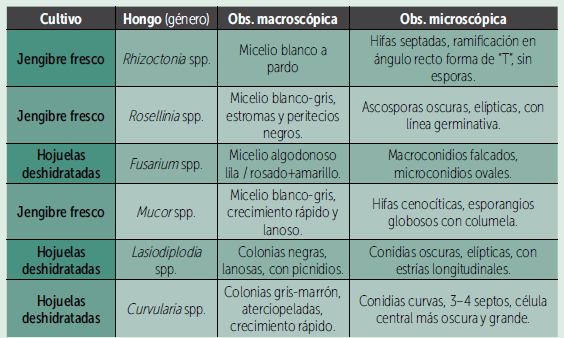
En las evaluaciones se identificó una comunidad fúngica asociada a rizomas de kion compuesta por Rhizoctonia spp., Rosellinia spp., Fusarium spp., Mucor spp., Lasiodiplodia spp. y Curvularia spp., siendo Rhizoctonia spp. y Rosellinia spp. los patógenos más probablemente vinculados al “moho blanco” y “moho negro” observado en poscosecha. En los ensayos in vitro, PERIMAX® (ácido peracético al 15 %) mostró una eficacia superior al 98 % de inhibición micelial de Rhizoctonia spp. a partir de 200 ppm, mientras que a 100 ppm se evidenció una menor sensibilidad de Rosellinia (37.1 % de inhibición) en comparación con Rhizoctonia (83.4 %). No obstante, a concentraciones de 300 ppm y superiores se alcanzó un control total (100 %) del crecimiento micelial en ambos aislados, lo que respalda el potencial de PERIMAX® como herramienta para el manejo preventivo de estos patógenos en poscosecha de kion.
Bibliografía
Choi, J.-H., Nah, J.-Y., Lee, M., Yim, S.- B., Jang, J. Y., Lee, T., & Kim, J. (2024). Fungal diversity in ginger and effect of storage conditions on occurrence of Fusarium and its mycotoxins. Food Control, 165, 110631. https://doi. org/10.1016/j.foodcont.2024.110631
Kaufman, S. (2016). Zingiber officinale (ginger). CABI Compendium, CABI Compendium, 57537. https://doi. org/10.1079/cabicompendium.57537
Zendrato, H. M., Masruchin, N., Nikmatin, S., & Wistara, N. J. (2024). Effective cellulose isolation from torch ginger stem by alkaline hydrogen peroxide – Peracetic acid system. Journal of Industrial and Engineering Chemistry, 131, 376-387. https://doi.org/10.1016/j.jiec.2023.10.040

Contacto:
Sebastián Iglesias Osores
Jefe IRD
+51 986 619 889
sebastian.iglesias@clenvi.pe
Luis Miguel Chávez
Zona Centro y Selva Central
+51 986 145 319







